news
新闻中心
康录生物与您相约中华医学会第十四次全国检验医学学术会议
会议时间:2018年9月5-8日
会议地点:大连世界博览广场
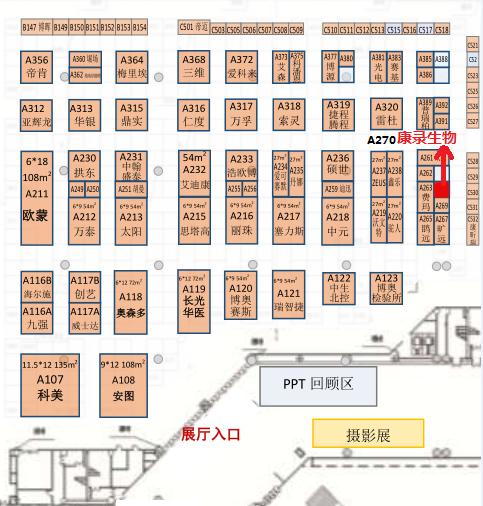
康录生物展位:A270
由中华医学会、中华医学会检验分会主办的中华医学会第十四次全国检验医学学术会议(简称2018全国检验医学大会)将于2018年9月5-8日在辽宁省大连市举行。这是中华医学会检验分会举办的大规模检验学界学术会议,也将是2018年度我国检验医学的一次盛会。本次会议将涵盖临床检验和实验室管理各领域最新的研究成果和发展趋势,并将对检验医学所面临的新形势和新挑战进行广泛充分的交流探讨。
本次会议中,武汉康录生物技术股份有限公司将携药物基因组学产品和快速FISH探针参展。
药物基因组学检测项目包含已获得CFDA III类医疗器械注册证的人类VKORC1和CYP2C9基因多态性检测试剂盒(PCR-荧光探针法)和人类CYP2C19基因多态性检测试剂盒(PCR-荧光探针法)两个产品,运用遗传信息指导个性化用药:正确的药物、正确的剂量、在恰当的时间、给予合适的患者。
已获证
人类CYP2C19基因多态性检测试剂盒(PCR-荧光探针法)
----国械注准20173403155
人类VKORC1 和CYP2C9 基因多态性检测试剂盒(PCR-荧光探针法)
----国械注准20173403154
2019年即将获证
人类SLCO1B1&ApoE基因多态性检测试剂盒(PCR-荧光探针法)
人类MTHFR基因多态性检测试剂盒(PCR-荧光探针法)
人类ALDH2基因多态性检测试剂盒(PCR-荧光探针法)
BCR/ABL融合基因检测试剂盒(PCR-荧光探针法)
PML/RARA融合基因检测试剂盒(PCR-荧光探针法)
AML1/ETO融合基因检测试剂盒(PCR-荧光探针法)
人类高血压五项检测试剂盒(PCR-荧光探针法)
人类CYSLTR1和GSDML基因多态性检测试剂盒(PCR-荧光探针法)
人类F5和PAI-1基因多态性检测试剂盒(PCR-荧光探针法)
人类TNF-α基因多态性检测试剂盒(PCR-荧光探针法)
人类GP IIIa/GP1BA/PEAR1基因多态性检测试剂盒(PCR-荧光探针法)
血液病快速FISH固相载体探针的多探针固相载体预置技术是康录生物研发的国内较早获得CFDA认证的多探针产品,极大满足了临床“便捷、高通量”的检测需求。其优势在于一次检测多个指标,独立分区,防止污染,采用固相载体探针预置技术,以更低的价格、更多的指标、更快的速度完成2小时快速杂交,操作简单,结果准确,兼容杂交仪。
血液病快速FISH固相载体探针产品目录
1.慢性淋巴细胞白血病染色体及基因异常检测试剂盒(原位杂交法)
| MYB/CEP6 | CEP12 | ATM/CEP11 | IGH/BCL2 |
| IGH | P53/CEP17 | IGH/CCND1 | D13S319/13q34 |
2.骨髓增生异常综合征染色体及基因异常检测试剂盒(原位杂交法)
| EGR1/D5S630 | PML/RARA | P53/CEP17 | RUNX1/RUNX1T1 |
| KMT2A(MLL) | D7S486/7q22.1-22.2 | CBFB/MYH11 | D20S108/20q13.12 |
3.急性淋巴细胞白血病染色体及基因异常检测试剂盒(原位杂交法)
| MYC | P16/CEP9 | E2A | 4q12/CEP10 |
| ETV6(TEL)/RUNX1(AML1) | KMT2A(MLL) | IGH | CEP17 |
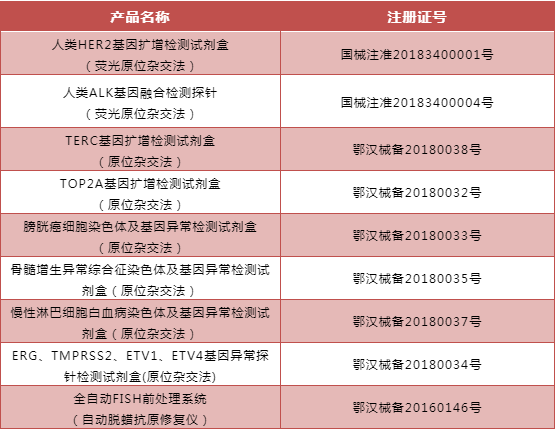
另外,人类HER2基因扩增检测试剂盒和人类ALK基因融合检测探针获得CFDA III类医疗器械注册证,是全球范围内较早投入临床检测市场的快速FISH探针,TOP2A、TERC、MDS、CLL及膀胱癌快速FISH检测探针,获得CFDA I类医疗器械注册备案证。
FISH产品线已有9种获得CFDA各级注册证
康录生物具有极强的科研实力,公司成立5年以来,自主研发各项技术已有13项获得国家发明专利,并有十余项专利在审。
武汉康录生物自成立伊始便以提供更高效的诊断产品为己任,坚持自主研发,以肿瘤、心脑血管疾病等重大疾病精准医疗诊断产品为战略方向,是一家集研发、生产、销售和检测服务为一体的高新技术企业。康录生物在此感谢广大新老客户对我们的信任与支持,在此诚挚邀请您莅临参观指导!
康录生物展位:A270